Evaluación Genética Detallada del Rendimiento Deportivo
La práctica regular de alguna actividad física es esencial para…
Sigue leyendo


Los trastornos mentales representan un desafío creciente para la salud pública global, afectando a millones de personas de todas las edades. Condiciones como la depresión, la ansiedad y los trastornos bipolares están entre las principales causas de discapacidad en el mundo, impactando significativamente la calidad de vida y las interacciones sociales.
En los últimos años, las investigaciones han explorado la conexión entre el microbioma intestinal y la salud mental, sugiriendo que la flora intestinal juega un papel crucial en la regulación del cerebro y el comportamiento, lo que abre nuevas perspectivas para la prevención y el tratamiento de estas condiciones.
Siga leyendo para descubrir cómo el microbioma intestinal y la depresión están relacionados, así como la influencia de este ecosistema en toda la salud mental.
La microbiota intestinal es un ecosistema dinámico que se forma junto con el organismo huésped, y está influenciada por las condiciones fisiológicas de dicho entorno. El microbioma, por su parte, corresponde al conjunto de todos los genes de una comunidad de microorganismos, representando el material genético total que compone la microbiota. Esto incluye el ADN de bacterias, virus, hongos y otros microorganismos que habitan en el intestino.
En este artículo de nuestro blog, abordamos las principales diferencias y detalles del microbioma y la microbiota intestinal.
Un microbioma intestinal diversificado está directamente relacionado con una buena salud. Este concepto de diversidad se refiere a la presencia de una amplia variedad de especies que coexisten en equilibrio. Cuanto más heterogéneo sea el microbioma, mayor será la variedad de funciones que los microorganismos desempeñan, contribuyendo al buen funcionamiento del cuerpo humano.
En el cuerpo humano, hay casi tantas células humanas como microbianas. Al analizar el microbioma, es importante recordar que cada una de las miles de especies presentes tiene su propio genoma. Así, la variedad de genes microbianos en nuestro cuerpo es mucho mayor que la de nuestros genes humanos. Estos genes microbianos producen sustancias que pueden impactar nuestra salud de manera positiva o negativa.
Un número creciente de enfermedades está asociado a alteraciones en el microbioma intestinal, y el mecanismo de esta relación surge del hecho de que los microorganismos pueden producir diferentes metabolitos biológicamente activos, y estos metabolitos pueden desempeñar un papel en el desarrollo de enfermedades.
Varios trastornos mentales y del desarrollo se han asociado con el microbioma intestinal. Además de un microbioma alterado, muchas personas con estas condiciones sufren de problemas gastrointestinales, como el síndrome del intestino irritable. Anteriormente, se creía que la depresión y la ansiedad eran la causa o contribuían a estos problemas, pero las investigaciones recientes sugieren lo contrario: la inflamación en el intestino puede influir en el desarrollo de trastornos mentales, como la depresión y la ansiedad.
La conexión entre el intestino y el cerebro se identificó al observar que los pacientes con trastornos mentales o del estado de ánimo, como la depresión, la ansiedad y la esquizofrenia, también presentaban desequilibrios en el microbioma intestinal (1). Además, las personas con síndrome del intestino irritable o enfermedades inflamatorias intestinales a menudo presentaban condiciones neurológicas (2), lo que dio lugar al concepto del “eje microbioma-intestino-cerebro” (3).
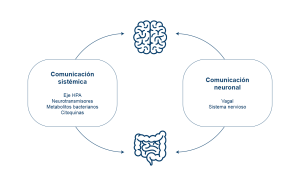
El eje intestino-cerebro es una red de comunicación bidireccional que integra funciones intestinales con los centros cognitivos y emocionales del cerebro. Este eje involucra los sistemas nervioso central, autónomo y entérico, así como los sistemas neuroendocrino, enteroendocrino y neuroinmune (4, 5).
Este eje desempeña un papel crucial al mediar los efectos de factores genéticos y ambientales en el desarrollo y funcionamiento del cerebro, y se ha asociado con la etiología de diversos trastornos psiquiátricos.
El sistema de comunicación se sustenta en varias vías, incluidas el nervio vago, el sistema endocrino intestinal, el sistema inmunológico y los metabolitos microbianos. Los ácidos grasos de cadena corta y neurotransmisores como el GABA, que son producidos y consumidos por los microorganismos intestinales, son ejemplos de metabolitos que influyen en este eje (6).
Los metabolitos pueden llegar al cerebro a través del nervio vago y la circulación sanguínea. El nervio vago conecta el cerebro con el colon y otros órganos, lo que permite que las moléculas del intestino influyan en el estado de ánimo, mientras que el cerebro también puede enviar señales de vuelta al intestino.
De esta manera, el eje intestino-cerebro no solo integra las funciones intestinales con las actividades cerebrales, sino que también demuestra cómo el equilibrio del microbioma intestinal puede impactar la salud mental y emocional.
La depresión es uno de los trastornos mentales más comunes. Aun así, sus causas siguen siendo parcialmente desconocidas y su diagnóstico es complejo.
Estudios recientes han demostrado variaciones características en el microbioma intestinal de personas con depresión, donde algunas bacterias implicadas son productoras de metabolitos como el glutamato, butirato, serotonina y ácido gamma-aminobutírico (GABA), sustancias con una potente acción neurológica. Estas sustancias pueden ejercer su efecto a través del nervio vago, que conecta el intestino con el cerebro, e influir en el estado de ánimo y la depresión (7).
La relación entre el microbioma intestinal y la depresión implica varios mecanismos complejos, tales como:
Estos mecanismos muestran cómo el microbioma intestinal puede desempeñar un papel importante en la regulación del estado de ánimo y la salud mental, sugiriendo que las intervenciones dirigidas a restaurar un microbioma saludable pueden tener un potencial terapéutico para la depresión.
La relación del microbioma intestinal con la salud mental es bidireccional, de modo que las alteraciones en la composición o funcionalidad del microbioma intestinal provocan cambios en la producción o disponibilidad de productos microbianos esenciales (18).
De igual manera, los estados emocionales como el estrés activarían la producción de hormonas como el cortisol, aumentando la permeabilidad intestinal y modificando la composición de la microbiota intestinal, favoreciendo la proliferación de especies proinflamatorias (19).
Se sabe que el estrés aumenta la permeabilidad intestinal, brindando así a las bacterias la oportunidad de translocarse a través de la mucosa intestinal y acceder directamente a las células inmunitarias y las células neuronales del sistema nervioso central. Esta es, por tanto, una vía potencial mediante la cual la microbiota puede influir en el SNC a través del sistema inmunológico y el sistema nervioso entérico en presencia de estrés.
El delicado equilibrio entre el microbioma humano y el desarrollo de psicopatologías es particularmente interesante dada la facilidad con que el microbioma puede ser alterado por factores externos, como la dieta (20), la exposición a antimicrobianos (21) o patrones de sueño interrumpidos (22), por ejemplo.
Estudios recientes han demostrado que la dieta es uno de los moduladores más importantes del eje microbioma-intestino-cerebro, ya que permite modificar la composición del microbioma y regular la producción de metabolitos microbianos con función clave (23). Esto es posible mediante intervenciones dietéticas basadas en el microbioma individual, dirigidas a la modulación de grupos microbianos o funcionalidades, promoviendo así una buena salud mental.
El microbioma intestinal de cada persona es único, formado por los microorganismos con los que hemos tenido contacto a lo largo de la vida, influenciado por el uso de antibióticos, genética, estilo de vida y alimentación (24).
Diversos estudios muestran que la dieta es un factor clave en la composición y funcionamiento del microbioma intestinal. Esto ocurre porque los nutrientes interactúan directamente con los microorganismos, favoreciendo o inhibiendo su crecimiento, según su capacidad de extraer energía de los alimentos (25).
Entre los nutrientes mejor aprovechados por el microbioma están los carbohidratos no digeribles, llamados glicanos, principalmente de origen vegetal, en los que estudios sugieren que una dieta rica en estos compuestos puede ayudar a mantener un microbioma equilibrado, además de promover la salud y aumentar la diversidad de bacterias (26).
Otra estrategia nutricional importante es el consumo regular de alimentos fermentados, que exponen al intestino a microorganismos beneficiosos. Un estudio reciente indica que una dieta rica en alimentos fermentados no solo aumenta la diversidad microbiana, sino que también puede reducir los marcadores inflamatorios en la sangre (27).
El desafío es cómo poner en práctica estas recomendaciones. Lo que realmente marca la diferencia para la salud es mantener un patrón alimentario equilibrado a largo plazo, sin centrarse únicamente en nutrientes específicos (28).
Además, la personalización de la dieta basada en el microbioma de cada persona es esencial, ya que cada uno responde de manera diferente a la alimentación. El objetivo final es desarrollar dietas personalizadas que mejoren o ajusten grupos microbianos específicos, aprovechando el potencial único de cada microbioma para promover la salud.
Un microbioma en desequilibrio, conocido como disbiosis, ocurre cuando hay una alteración en la composición o función de los microorganismos intestinales. Este desequilibrio puede corregirse con el consumo de prebióticos y/o probióticos. Los prebióticos son alimentos ricos en fibra que promueven el crecimiento de bacterias beneficiosas en el intestino.
Al añadir diferentes tipos de prebióticos a la dieta y reducir alimentos que favorecen microorganismos potencialmente perjudiciales (como aditivos y proteínas en exceso), podemos reequilibrar el microbioma, proporcionando los nutrientes necesarios para el aumento de bacterias saludables.
Además de la alimentación, el estilo de vida es fundamental para mantener el equilibrio del microbioma intestinal. Reducir el estrés, tener una buena calidad de sueño y practicar ejercicio son factores que contribuyen directamente a este equilibrio.
Para restaurar el microbioma de manera eficaz, es esencial entender su estado actual y cómo está impactando la salud. Para ello, un examen con alta cobertura y resolución, que ofrezca información detallada sobre el comportamiento de los microorganismos intestinales, es indispensable.
SYNLAB ofrece el examen MyBiome, una prueba exclusiva que analiza el microbioma intestinal mediante secuenciación masiva (shotgun metagenomics), proporcionando una lectura completa del genoma de los microorganismos intestinales. MyBiome ofrece:
MyBiome ofrece información detallada sobre los microorganismos intestinales y su impacto en la salud, con aplicación clínica directa.
MyBiome está especialmente indicado para:
La realización de exámenes precisos y actualizados es esencial para realizar diagnósticos más acertados y para guiar mejor los tratamientos. SYNLAB está aquí para ayudarte.
Ofrecemos soluciones diagnósticas con estricto control de calidad a las empresas, pacientes y médicos que atendemos. Estamos en Brasil hace más de 10 años, operamos en 36 países y tres continentes, y somos líderes en la prestación de servicios en Europa.
Ponte en contacto con el equipo de SYNLAB y conoce los exámenes disponibles.
Referencias Bibliográficas
La práctica regular de alguna actividad física es esencial para…
Sigue leyendo
El Síndrome de Sobrecrecimiento Bacteriano en el Intestino Delgado (SIBO)…
Sigue leyendo
Los trastornos mentales representan un desafío creciente para la salud…
Sigue leyendo